2024年吉林省長春市寬城區中考化學一模試卷
發布:2025/7/5 1:0:10
一、選擇題(每小題只有一個選項符合題意。每小題1分,共10分)
-
1.規范的操作是確保實驗成功的關鍵,下列所示的操作正確的是( )
A. 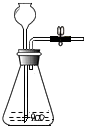
檢查裝置氣密性B. 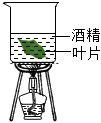
脫色處理C. 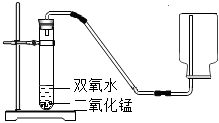
制取并收集氧氣D. 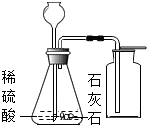
實驗室制取二氧化碳組卷:3引用:0難度:0.5 -
2.化學學科的特征是從微觀層面認識物質。對下列做法或說法解釋正確的是( )
A.鐵質水龍頭表面鍍鉻可防銹——改變了金屬的內部結構 B.攪拌能加快蔗糖在水中的溶解——攪拌增加了蔗糖在水中的溶解度 C.金剛石和石墨的物理性質差異很大,是因為碳原子的排列方式不同 D.純堿溶液呈堿性——純堿是由Na+和OH構成 組卷:16引用:2難度:0.5 -
3.無錫留青竹刻是無錫眾多非物質文化遺產之一,下列制作步驟中涉及化學變化的是( )
A.采伐竹材 B.旺火煮青 C.晾曬陰干 D.留青雕刻 組卷:134引用:11難度:0.8 -
4.學會識圖能發展科學思維。下列圖像與反應過程的變化趨勢對應正確的有( )
序號 ① ② ③ ④ 圖像 
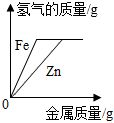


反應過程 KMnO4受熱分解 向含等質量HCl的稀鹽酸中分別加入Zn和Fe至過量 向NaOH溶液中逐滴加入稀鹽酸至過量 木炭在充滿O2的集氣瓶中燃燒 A.1個 B.2個 C.3個 D.4個 組卷:48引用:2難度:0.5 -
5.下列對實驗現象的描述,錯誤的是( )
A.用一氧化碳還原氧化銅實驗時,黑色固體慢慢變紅,產生使澄清石灰水變渾濁的氣體 B.硫在氧氣中燃燒產生明亮的藍紫色火焰,生成無色有刺激性氣味的氣體 C.鐵絲在氧氣中劇烈燃燒,火星四射,生成一種紅色固體 D.向硫酸銅溶液中滴加氫氧化鈉溶液會生成藍色絮狀沉淀 組卷:40引用:2難度:0.6 -
6.下列化學用語正確的是( )
A.氫單質的化學式H B.氦氣的化學式He C.鎂的元素符號mg D.三氧化二鐵的化學式2Fe3O 組卷:6引用:2難度:0.9 -
7.第24屆冬季奧運會將于2022年2月4日在我國北京市和張家口市聯合舉行。“綠色”成為即將到來的北京冬奧會的主要理念。下列建議中不可取的是( )
A.使用可降解塑料袋 B.推廣露天焚燒垃圾 C.積極參與植樹造林 D.改進尾氣凈化技術 組卷:31引用:6難度:0.5 -
8.火箭發動機里使用的液態氧的作用是( )
A.火箭燃料 B.火箭助燃劑 C.供宇航員呼吸 D.汽化吸熱 組卷:104引用:3難度:0.7 -
9.硫酸鐵銨[NH4Fe(SO4)2]是一種分析試劑,測定鹵素時常用作指示劑。下列說法中正確的是( )
A.硫酸鐵銨屬于氧化物 B.硫酸鐵銨中氫元素的質量分數最小 C.硫酸鐵銨中鐵元素為+2價 D.硫酸鐵銨由1個氮原子、4個氫原子、1個鐵原子、2個硫原子和8個氧原子構成 組卷:17引用:4難度:0.7 -
10.下列數據為常見水果的近似pH,其中呈堿性的是( )
A. 
柿子pH=8.5B. 
菠蘿pH=5.1C. 
蘋果pH=4.1D. 
楊梅pH=2.5組卷:9引用:4難度:0.9
二、非選擇題(化學方程式2分,其它每空1分,共40分)
-
11.用化學用語填空:
(1)2個氫原子;
(2)硫酸根離子;
(3)寫出三氧化二鐵的化學式并標出該化合物中鐵元素的化合價.組卷:1引用:1難度:0.9 -
12.某鄉的村民普遍患有一種奇怪的疾病,脫發、失明甚至死亡.經中國科學院地化所專家對該地區水源、植物進行了分析,確定引起疾病的原因是附近礦山亂挖濫采,使水源中鉈(T1)元素含量過高所致.
(1)為使當地民眾擺脫困境,當務之急應采取的措施是.
(2)高純鉈及其合金可作半導體材料,價格可與黃金相當.寫出使硫酸亞鉈轉化為純鉈的化學方程式.
Tl2SO4(溶液)→TlOH(溶液)→蒸干→TlO2TlH2,,.組卷:32引用:2難度:0.5 -
13.(1)甲圖是一種“化學氧自救器”,主要用于煤礦井下應急。它利用人呼出的二氧化碳與自救器藥罐中的生氧劑(超氧化鉀KO2)接觸產生氧氣,該反應的化學方程式為:4KO2+2CO2═2X+3O2,則X的化學式是
。
(2)若要在實驗室制取并收集一瓶氧氣,你準備選擇乙圖裝置中的(填編號),其相應的化學方程式。組卷:5引用:4難度:0.3 -
14.浩瀚的大海里蘊藏著豐富的資源,開發海水資源前景廣闊。湛江海洋研究所以含有CaCl2、MgCl2的鹵水和貝殼(主要成分為CaCO3)為主要原料在實驗室制備無水CaCl2,流程如圖1所示。

請回答下列問題:
(1)操作I中,用到的玻璃儀器有燒杯、玻璃棒、。
(2)以MgCl2為例,寫出鹵水中除去Mg2+時發生反應的化學方程式:。
(3)操作Ⅱ中,酸化時應選擇的酸是(填化學式)。
(4)上述反應中未涉及的基本反應類型是(填字母)。
a.復分解反應b。置換反應c。化合反應d。分解反應
(5)回收的CO2在紫外線照射和催化劑作用下能與水蒸氣反應,生成甲烷和氧氣,該反應的化學方程式為。紫外線照射時,在不同催化劑(①、②、③)的作用下,甲烷產量隨光照時間的變化如圖2所示,在第10小時甲烷產量最高的是(填“①”“②”或“③”)。組卷:19引用:1難度:0.5 -
15.水是生命之源,水在生活中發揮著很重要的作用。某校化學興趣小組的同學們在學習了與水有關的知識后進行了一系列探究。
任務一:了解自來水廠生產自來水的過程
【調查了解】同學們在老師的帶領下到當地自來水廠參觀自來水的生產過程,了解到自來水的生產過程如圖所示。
【分析交流】生產自來水的過程中可加入的絮凝劑是,其凈水原理為。
任務二:測量自來水的硬度
【查閱資料】同學們查閱了相關資料,了解到國家有關水的硬度的標準為:
【進行測量】同學們在實驗室中取少量自來水,用便攜式水硬度檢測儀測得該自來水的硬度為311.2mg/L,說明本地區的自來水屬于類別 極軟水 軟水 中硬水 硬水 高硬水 以CaCO3濃度計/(mg/L) 0~75 75~150 150~300 300~450 450~700 。同學們又向此自來水中加入少量肥皂水,攪拌后觀察到,也得出了相同結論。
【交流討論】水的硬度是一項重要的指標。日常生活中常用的方法來降低水的硬度。
任務三:檢驗水垢與醋酸反應后氣體的成分
【查閱資料】同學們查閱了相關資料,了解到水垢的主要成分中有CaCO3,加入醋酸后會產生CO2氣體。
【進行探究】同學們收集了一瓶水垢與醋酸反應產生的氣體并設計實驗證明該氣體是CO2,實驗報告如下:
任務四:自制簡易凈水器實驗步驟 實驗現象 實驗結論 該氣體是CO2 
【交流探討】同學們認為,雖然自來水的水質在出廠時已檢驗合格,但在管道運輸過程中仍不可避免地受到污染,所以在家中使用自來水時,最好安裝凈水器。于是他們在老師的幫助下,利用所學知識,制作了簡易凈水器,請你與他們一同完成。其中,石英砂起作用。組卷:27引用:1難度:0.7 -
16.某校學習小組學習固體、液體的密度測量之后,準備探究氣體密度的測定。學習小組認為氣體密度的測定原理和小石塊、鹽水的密度測定一樣。
【提出問題】
如何利用石灰石與稀鹽酸反應來測定生成CO2的質量和體積,并處理數據。
【實驗設計】通過下列兩個實驗分別測定CO2的質量和體積:
【分析與表達】
(1)實驗Ⅰ中,將小燒杯中的10ml稀鹽酸加入到盛有石灰石的大燒杯中,并不斷攪拌,直至不再產生氣泡,發生反應的化學方程式為。
(2)實驗Ⅱ中,裝好藥品前先(填操作名稱),然后,最后將10ml稀鹽酸快速推入燒瓶中。若稀鹽酸是緩慢推入的,則可能造成的后果是。
【記錄與處理】
(3)實驗產生的CO2質量為實驗Ⅰ中反應前的電子天平示數與完全反應后的示數差
(4)實驗Ⅱ的實驗記錄如下(表中數據在相同溫度、相同壓強條件下測定):
根據以上實驗過程和數據綜合分析,最終生成CO2的體積是時間/min 1 2 3 4 5 6 7 8 9 10 注射器讀數/ml 60.0 85.0 88.0 89.0 89.5 89.8 89.9 90.0 90.0 90.0 ml。
(5)根據(3)、(4)測得的數據,用密度的計算公式計算。
【實驗反思】
(6)有同學認為實驗Ⅰ與Ⅱ中鹽酸以及石灰石的用量不僅要一樣,而且石灰石要完全反應。對于實驗Ⅰ與實驗Ⅱ中鹽酸以及石灰石的用量要一樣大家都贊同,但對于反應中應該石灰石過量才不會影響實驗結果有不同的看法,你的看法是:。組卷:29引用:1難度:0.3 -
17.如圖分別是水蒸氣液化,水通電分解和氫氣在氯氣中燃燒的微觀變化示意圖。請回答下列問題:
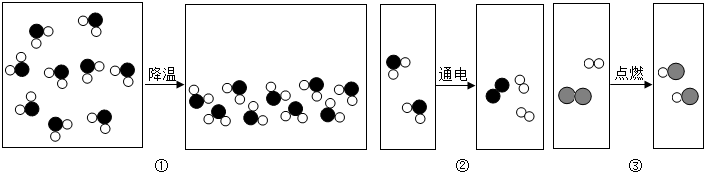
(1)圖②表示的反應符號表達式是;
(2)從微觀的角度解釋圖①、圖②的本質區別是;
(3)由圖②、圖③可得到:保持水的化學性質的最小粒子是,在化學變化中一定不變的粒子是,可能發生改變的是分子的;
(4)由圖③還能獲得的一條信息是。組卷:56引用:11難度:0.5 -
18.分類、類比是學習化學的重要方法。
(1)化學是一門以實驗為基礎的科學,下面是我們在初中化學課中經歷過的實驗。若按實驗中發生的主要化學反應的基本反應類型進行分類,應將實驗歸為一組(填字母),你的分類依據是。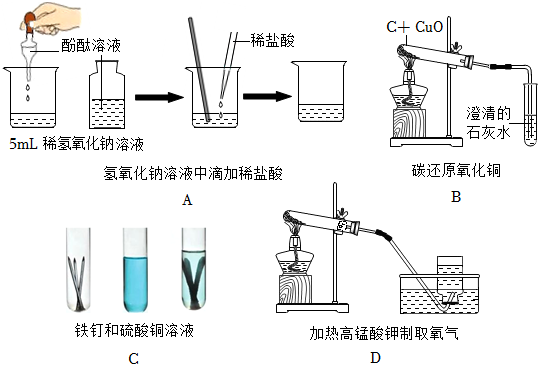
(2)經過對實驗B中氧化劑和還原劑中的某元素的化合價在化學反應前后的變化進行分析,請你猜想Fe+CuCl2=Cu+FeCl2反應中,氧化劑是(填化學式),請你大膽總結一下,在反應中化合價的物質通常做還原劑。組卷:5引用:1難度:0.8 -
19.為測定某碳酸氫銨化肥中的含氮量,某同學在實驗室里取用8.5g該化肥樣品與15gNaOH溶液放入燒杯中共熱,恰好完全反應(樣品中雜質不與堿反應,也不溶于水),生成的氨氣全部逸出后,測得燒杯中殘留物為21.8g (反應的化學方程式為NH4HCO3+2NaOH
Na2CO3+2H2O+NH3↑).試求:△
(1)生成氨氣的質量.
(2)該化肥中氮元素的質量分數(計算結果精確到0.1%).
(3)所得溶液中溶質的質量分數(計算結果精確到0.1%).組卷:5引用:1難度:0.3


